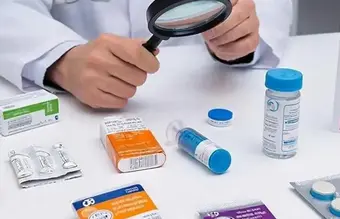
Средство измерений
Каждое медицинское изделие (далее – МИ) проходит стадию испытаний при государственной регистрации. Одним из них являются испытания в целях утверждения типа средств измерений (далее – типа СИ).
Средство измерений (далее – СИ) – техническое средство, предназначенное для измерения, имеющее нормированные метрологические характеристики, воспроизводящее и (или) хранящее единицу физической величины, размер которой предполагается неизменным (в пределах установленной погрешности) в течение известного интервала времени.
Рисунок 1 – Пример средства измерения «Температурный индикатор для контроля параметров холодовой цепи»
Список измерений при осуществлении деятельности в здравоохранении представлен в Постановлении Правительства РФ от 16 ноября 2020 г. N 1847 «Об утверждении перечня измерений, относящихся к сфере государственного регулирования обеспечения единства измерений». Наиболее распространенными измерениями являются: измерение температуры тела человека контактным методом (электронный термометр), измерение веса и роста пациента (весы медицинские напольные с ростомером), измерение оптико-физических характеристик наборов пробных очковых линз, неинвазивное измерение артериального давления (тонометр).
Испытания в целях утверждения типа средств измерений
Тип средств измерений – совокупность средств измерений, предназначенных для измерения одних и тех же величин.
Рисунок 2 – Схема проведения испытаний в целях утверждения типа СИ.
Этап 2. Подготовка пакета документов
После выбора испытательной лаборатории производитель или уполномоченный представитель производителя предоставляет в лабораторию следующий комплект документов:
1) Заявка на проведение испытаний в целях утверждения типа средств измерений;
2) Руководство по эксплуатации;
3) Доверенность от производителя на уполномоченного представителя производителя;
4) Фотоизображения каждой модели изделия.
Лаборатория анализирует эти документы и указывает стоимость испытаний. Стоимость испытаний зависит от объема и параметров испытаний. После оплаты испытаний, производитель или уполномоченный представитель производителя предоставляет в лабораторию образцы всех моделей МИ, которые планируются к регистрации.
Этап 3. Согласование программы испытаний
После получения образцов лаборатория составляет программу испытаний, которая включает:
1. Объект испытаний;
2. Содержание и объем испытаний;
3. Методы (методики) испытаний;
4. Условия испытаний;
5. Количество представляемых на испытания серийно изготовленных образцов средств измерений;
6. Алгоритмы обработки результатов, полученных в ходе испытаний.
Важно: если изделие включает в себя несколько видов измерений, например, монитор пациента (измерение температуры тела, измерение артериального давления, измерение объема вдыхаемого/выдыхаемого воздуха), то необходимо описать порядок проведения испытаний для каждого параметра измерения.
Этап 4.1. Проведение испытаний
После согласования программы, лаборатория приступает к испытаниям изделия. При успешном прохождении испытаний лаборатория выдает следующий комплект документов:
1. Проект описания типа СИ;
2. Методика поверки;
3. Акт, программа и протокол испытаний.
Если по результатам испытаний изделие не соответствует заявленной точности, лаборатория запрашивает образцы из новой партии или устраняет неисправность в уже предоставленных образцах.
Этап 4.2. Проведение испытаний и выдача документов для РЗН
Процесс испытаний аналогичен пункту 4.1, но на этом этапе испытания СИ могут быть завершены без утверждения типа СИ и внесения в систему «АРШИН». Акт, программа и протокол предоставляются РЗН.
Этап 5. Проведение экспертизы во ФГБУ «ВНИИМС
После этапа 4.1 комплект документов передается во ФГБУ «ВНИИМС», который проводит экспертизу полученных материалов и по результатам готовит заключение результатов испытаний. В случае замечаний от ФГБУ «ВНИИМС» документы направляются на доработку. После доработки процесс повторяется.
Этап 6. Внесение данных в систему «АРШИН»
При положительном заключении комплект документов передается в Росстандарт По желанию, производитель может запросить бумажную версию сертификата. Весь процесс испытаний и внесения во ФГИС «АРШИН» занимает 4-6 месяцев в зависимости от объема работ. Параллельно с внесением в госреестр, акт, программа и протокол могут быть представлены РЗН в составе регистрационного досье.

Рисунок 4 – Варианты проведения испытаний
Этап 7. Поверка средств измерений
Перед выпуском в обращение изготовленной и ввезенной партии продукции ее необходимо направить на первичную поверку. Поверка средств измерений — это определение метрологическим органом погрешностей средств измерений (или проверка их соответствия допускаемым нормам) и установление их пригодности к применению. Поверка проводится для партии медицинских изделий в соответствии с установленной методикой поверки, в аккредитованной испытательной лаборатории.
Различают первичную и вторичную (повторную) поверку средства измерений. Первичная поверка – это испытание нового средства измерений или после ремонта, технического обслуживания, регулировки, а также при ввозе средства измерений из-за рубежа для реализации. Вторичная поверка – это процедура, проводимая над средствами измерений, находящимися в эксплуатации или на хранении, после установленных для средства измерений межповерочных интервалов. По результатам поверки во ФГИС «АРШИН» вносится каждый Серийный номер изделия из поверенной партии.
- Российская Федерация. Правительство. «Об утверждении перечня измерений, относящихся к сфере государственного регулирования обеспечения единства измерений»: Постановление Правительства РФ от 16 ноября 2020 г. № 1847 (с изменениями и дополнениями)// Официальный интернет-портал правовой информации;
- Федеральной службы по аккредитации.